Novo mecanismo de ação de complexos de cobre contra melanoma é revelado
Metalodrogas antitumorais vêm despertando crescente interesse nos últimos anos, mas, por causarem efeitos adversos, ainda representam um desafio para os cientistas. Um exemplo são os compostos de platina usados como quimioterápicos contra diversos tipos de câncer, que provocam intensos efeitos colaterais, além de resistência celular ao tratamento. Por isso a importância do desenvolvimento de fármacos alternativos, baseados em diferentes compostos metálicos, como os complexos de cobre(II) com ligantes imínicos sintetizados, caracterizados e estudados como agentes antitumorais contra o melanoma pelo grupo da professora Ana Maria da Costa Ferreira, do Instituto de Química da USP e do CEPID Redoxoma.
Em novo estudo, recentemente publicado no jornal Chemico-Biological Interactions, os pesquisadores mostram que o complexo de cobre(II) dinuclear é mais citotóxico para células de melanoma SKMEL-05 e SKMEL-147 do que o complexo mononuclear análogo e que esse efeito é estimulado pela radiação ultravioleta B (UVB), que induz a formação de melanina. Os resultados do trabalho ampliam dados obtidos pelo grupo anteriormente, ao indicar diferentes mecanismos de ação de tais complexos, dependendo de sua nuclearidade. Segundo os autores do artigo, os complexos de cobre dinucleares podem constituir uma nova abordagem terapêutica contra o melanoma.
“Estudamos complexos de cobre mono e dinucleares desde o mestrado da Cléia Justino Nunes e os novos resultados foram obtidos em seu doutorado — ela é a primeira autora do artigo. Ambos os complexos são reativos contra células de melanoma, mas o dinuclear, que tem dois centros de cobre em sua estrutura, tem uma reatividade muito maior, não é apenas o dobro da reatividade do mononuclear análogo. A diferença entre eles está no mecanismo de ação e isto nos levou a investigar a relação entre estrutura e reatividade. O complexo dinuclear age por reações dieletrônicas, ou seja, por transferência de dois elétrons, de forma similar às enzimas tirosinases, que catalisam a formação de melanina”, afirmou a pesquisadora.
O melanoma é o tipo mais perigoso de câncer de pele. É agressivo, metastático, com alta fatalidade se diagnosticado tardiamente e com frequência é resistente às terapias usuais. Ele surge a partir da transformação maligna dos melanócitos, que são células localizadas na barreira entre a epiderme e a derme responsáveis pela síntese de melanina, o pigmento que dá coloração à pele, olhos e cabelos. A melanina tem um papel dual anti e pró-oxidante. Além de conferir proteção à pele contra raios UVB, ela também pode ter um efeito nocivo, pois é capaz de coordenar íons metálicos, principalmente ferro e cobre, participando de reações que geram espécies reativas.
Compostos de cobre mononucleares usualmente atuam como agentes redox contra tumores, danificando biomoléculas e organelas via formação de espécies reativas de oxigênio. Os compostos dinucleares têm outros modos de ação, apesar de alguns deles também agirem por vias mediadas por espécies reativas tendo por alvo as mitocôndrias. Por exemplo, algumas espécies descritas na literatura atuam como nucleases que contêm metal, quebrando ligações fosfato em ácidos nucleicos (DNA e RNA); outras, com diferentes ligantes, agem como inibidores de telomerase humana, da transcriptase reversa de HIV e de outras polimerases; outros complexos podem ainda bloquear a síntese de DNA.
Dados ampliados
Em um trabalho anterior do grupo, a atividade maior de complexos dinucleares de cobre(II) contra o melanoma em comparação com complexos mononucleares já havia sido detectada, mas os compostos estudados tinham o DNA como alvo, por um mecanismo oxidativo. O estudo também indicava uma correlação entre o conteúdo de melanina e a sensibilização das células, principalmente quando tratadas com o composto dinuclear.
Agora, os pesquisadores confirmaram e ampliaram os dados. Em colaboração com o grupo do oncologista Roger Chammas, do Instituto do Câncer da Faculdade de Medicina da USP (ICESP), eles avaliaram a citotoxicidade dos complexos de cobre(II) mono e dinucleares nas linhagens de células de melanoma humano SKMEL-05 e SKMEL-147, após 24 e 48h de incubação, e constataram que o complexo dinuclear causa mais danos aos tumores. Testes clonogênicos, usados para avaliar a proliferação celular, igualmente indicaram maior atividade deste composto, com diminuição significativa do número de células sobreviventes após o tratamento. Tanto os compostos mononucleares como dinucleares são capazes de formar espécies radicalares.
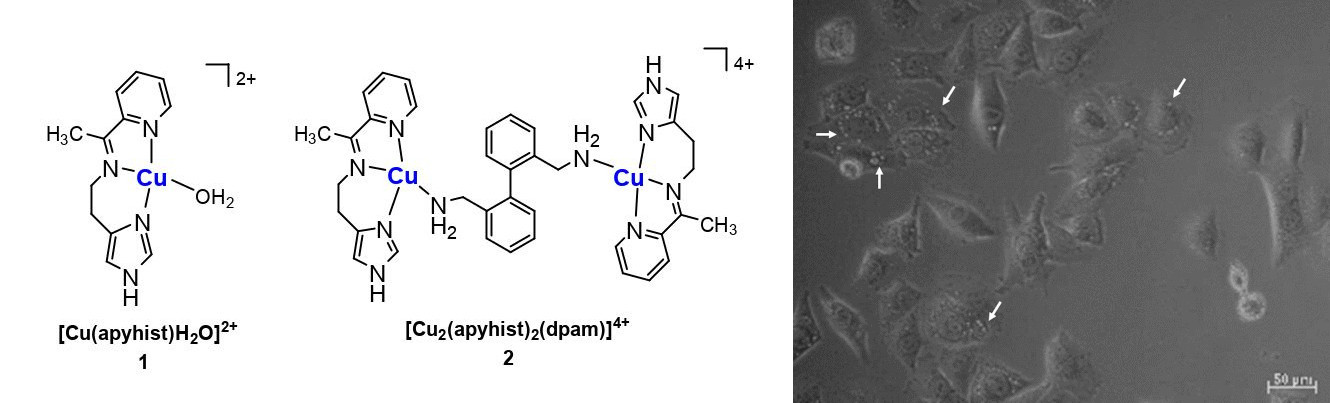
Esquerda: estrutura dos complexos de cobre(II); Direita: Células de melanoma SKMEL-05 após exposição à luz UVB e depois tratadas por 24h com o complexo dinuclear. As setas indicam o acúmulo de vacúolos citoplasmáticos
Imagens: Ana Maria da Costa Ferreira/Andréia Hanada Otake
No estudo foi testada ainda a influência da radiação UVB e os pesquisadores viram que apenas na presença do complexo dinuclear a exposição das células à radiação aumentou os danos. Eles também observaram que células de melanoma com maior concentração de melanina são mais sensíveis ao complexo. “A irradiação faz com que as células produzam mais melanina. O complexo dinuclear é mais eficientemente reduzido pela melanina do que o mononuclear, disparando o ciclo catalítico oxidativo com formação de espécies reativas de oxigênio, desta forma sensibilizando mais as células com mais melanina”, explica Costa Ferreira.
Para saber como os compostos causam a morte celular, os pesquisadores fizeram ensaios de autofagia, que mostraram o aumento do nível de vacúolos citoplasmáticos após o tratamento com o complexo dinuclear, e mediram as proteínas marcadoras de autofagia LC3, que também estavam aumentadas. “Vimos que as células tumorais incubadas com o complexo dinuclear de cobre morrem por dois processos: por apoptose, que é a morte programada, e também por autofagia, que é uma morte na qual a célula se recicla”, disse a pesquisadora.
Os resultados da pesquisa também mostraram que o efeito tóxico dos compostos em células não tumorais foi insignificante, indicando que os complexos apresentam seletividade para células tumorais pigmentadas. Eles avaliaram esse efeito em queratinócitos, que representam 80% das células epidérmicas.
Metalodrogas de cobre
O cobre é um metal essencial, que está presente em proteínas de diversos organismos e participa de importantes reações biológicas. Seres humanos têm concentração de cobre de 1,7 mg/kg corpóreo, inserido no sítio ativo de muitas proteínas e enzimas. Ele é obtido por meio da alimentação e sua homeostase é bem controlada, pois tanto o excesso quanto a falta de cobre causam problemas de saúde.
Para Costa Ferreira, por já estarem presentes no organismo, esses metais essenciais são candidatos preferenciais para o desenvolvimento de metalodrogas, que são medicamentos com pelo menos um centro metálico. No entanto, como o cobre é muito reativo, as metalodrogas baseadas neste metal sempre foram consideradas tóxicas. Para a pesquisadora, a maior reatividade dos metais é uma característica positiva, pois abre mais possibilidades de ligações químicas, e a toxicidade pode ser regulada pelos ligantes. “Devido à reatividade, a concentração de cobre livre nas células é muito baixa (<10-10 mols/L). Ele está sempre coordenado a biomoléculas, justamente para modular sua atividade. Nos complexos metálicos, os ligantes podem modular, isto é, modificar e controlar a atividade biológica do metal. Nossos ligantes são planejados para prover características desejadas ao íon metálico, é dessa forma que podemos modular a atividade do cobre. Todos esses compostos que fazemos são muito estáveis, eles não rompem a ligação com o íon metálico facilmente — o metal está sempre ligado ao ligante e é assim que entra nas células”, explica.
Outra vantagem dos complexos metálicos, segundo a pesquisadora, é serem multifuncionais, agindo em diversas moléculas. “Os compostos de cobre, por exemplo, também inibem quinases, que são proteínas bastante abundantes e que controlam ciclos celulares, inclusive de tumores”.
O grupo de Costa Ferreira também está testando os complexos em matrizes de sílica funcionalizada. “Ter um material para liberação do composto seria uma possibilidade para tratamento tópico de tumores”. O próximo passo será testar os efeitos dos complexos de cobre(II) em diferentes melanomas em peles artificiais.
O artigo Unlike reactivity of mono- and binuclear imine-copper(II) complexes toward melanoma cells via a tyrosinase-dependent mechanism, de Cléia Justino Nunes, Andréia Hanada Otake, Silvina Odete Bustos, Rodrigo Boni Fazzi, Roger Chammas e Ana Maria da Costa Ferreira, pode ser lido aqui.
